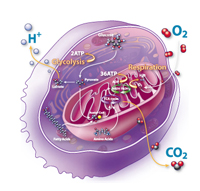
幹細胞から増殖させた3次元細胞培養のサブタイプであるオルガノイドは、生体内臓器を模倣し、in vivoの生理機能や病態⽣理を忠実に再現することができます。そのため、⽣物学的研究や疾患メカニズムの解明、創薬研究等において、従来の2次元培養細胞ベースのアッセイとは異なる有用性を提供します。
細胞外フラックスアナライザーXFでは、2次元培養細胞だけでなく、オルガノイドやスフェロイドのような3次元培養細胞、組織片や小さな胚などを用いたエネルギー代謝測定を行うことも可能です。
妊娠中の母親のアルコール曝露は、胎児の発育に大きな影響を与え、認知機能障害や精神障害など、胎児性アルコールスペクトラム障害(FASD)として知られるさまざまな症状を引き起こしますが、その病態生理やメカニズムはほとんど分かっていません。最近開発された人工多能性幹細胞からのヒト大脳オルガノイドは、発生や構造の面で胎児の脳に類似しており、動物モデルよりもFASD研究に適したin vitroシステムの開発が可能です。
本研究では、ヒト大脳オルガノイドを用いて暴飲暴食をモデル化し、アルコール(エタノール)によってオルガノイド内の神経病理学的表現型とシグナル伝達経路にもたらされる下流の毒性作用を定量化することを試みました。その結果、アルコールに曝露されたオルガノイドは、細胞レベル、細胞内レベル、生体エネルギー代謝レベル、遺伝子発現レベルで不健康になることが明らかになりました。
アルコールに曝露されたオルガノイドは、ミトコンドリアの機能障害と代謝ストレスを引き起こし、(1)基礎呼吸、ATP産生、プロトンリーク、最大呼吸、予備呼吸能に関連するミトコンドリア酸素消費速度の低下、(2)アルコール処理したオルガノイドは、コントロールと比較してミトコンドリアによらない呼吸が増加しました。また、解析した17,195遺伝子のうち199遺伝子の発現に影響を及ぼすことがわかり、これらの発現異常遺伝子の多くが神経の発達や神経系の生理学、神経変性に関与しているものでした。
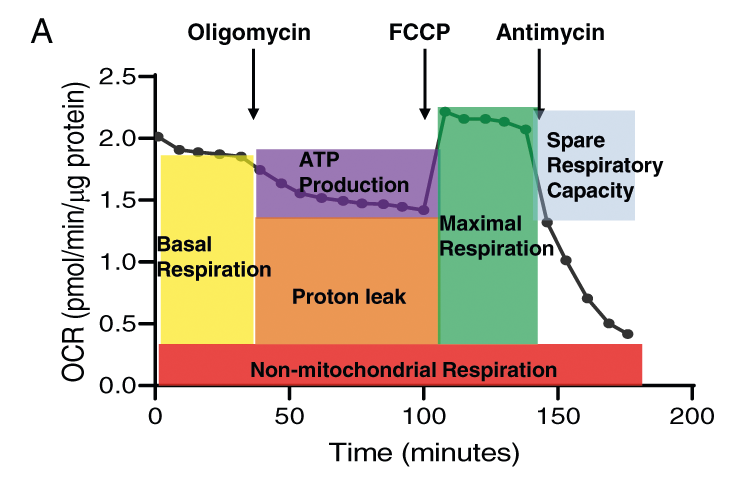
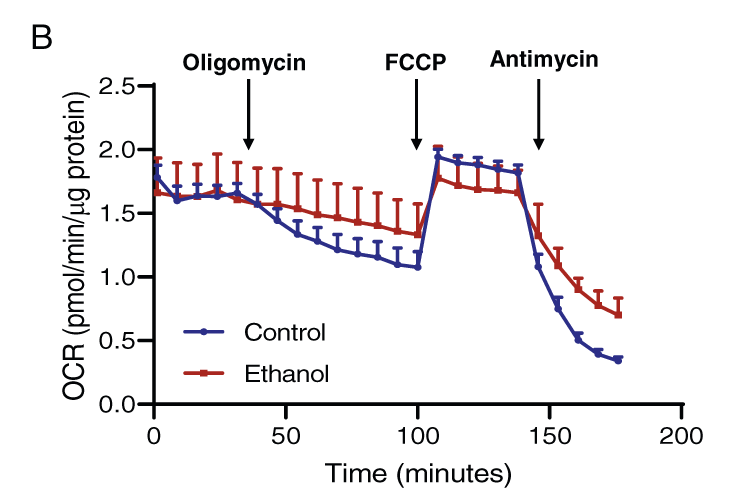
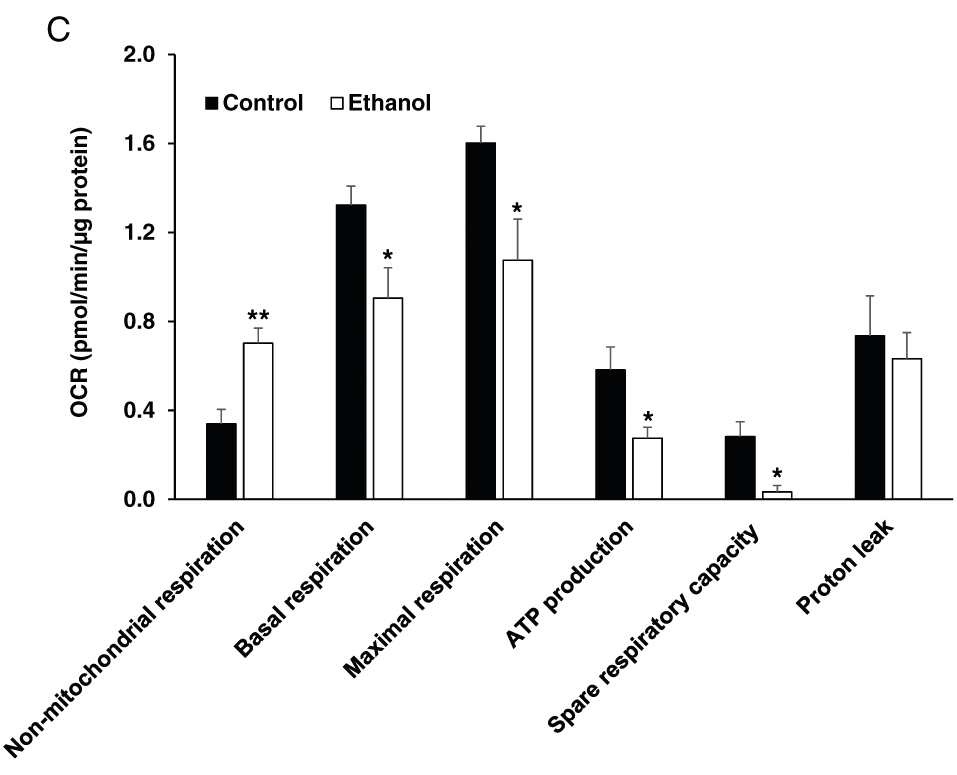
Figure: iPSC株1由来脳オルガノイドのミトコンドリア呼吸能に及ぼすエタノール(230 mg/mL、6時間)の影響。A:10μMオリゴマイシン(ATP合成酵素阻害剤)、10μMカルボニルシアニド-4-(トリフルオロメトキシ)フェニルヒドラゾン(FCCP;ミトコンドリアにおける酸化的リン酸化の阻害剤)、および10μMアンチマイシンA(複合体IIIを阻害することによる電子伝達系遮断剤)を順次投与した後の脳オルガノイドの酸素消費速度(OCR)のトレースを示す。B:コントロールと230mg/dLエタノール処理した大脳オルガノイドのオリゴマイシン、FCCP、アンチマイシンAに対する6時間のOCRトレース。C:エタノール処理脳オルガノイドのミトコンドリア機能を表すOCRパラメーター(基礎呼吸、ATP産生、最大呼吸、予備呼吸能)は、エタノール曝露後に有意に減少し、ミトコンドリアによらない呼吸は増加した。
Reference: Modeling alcohol-induced neurotoxicity using human induced pluripotent stem cell-derived three-dimensional cerebral organoids
Arzua et al., Translational Psychiatry (2020) 10:347 https://doi.org/10.1038/s41398-020-01029-4 (

)
前立腺炎や前立腺肥大症(BPH)などの一般的な前立腺疾患は、年齢に関係なく発症率が高いです。活性酸素種(ROS)や慢性炎症などの細胞ストレスは、前立腺肥大やがんの進行・発生に関与しています。カエンフェロール(Kaempferol)は、ブロッコリーやホウレンソウなど様々な植物に豊富に含まれるフラボノイドの一種で、抗酸化作用や抗炎症作用などの生理活性を示すことが報告されています。
本研究では、前立腺オルガノイドを導入し、様々な細胞ストレスに対するカエンフェロールの保護作用を調べました。
COX-2、iNOS、炎症性サイトカインであるp-IκBおよび活性酸素のレベルは、LPS(リポ多糖)処理により上昇しましたが、カエンフェロール処理により逆転しました。カエンフェロールは、Nuclear factor erythroid 2-related factor 2(Nrf2)関連経路を活性化し、ミトコンドリアの品質管理タンパク質であるPGC-1α、PINK1、Parkin、Beclinを増強しました。LPSによって誘導されたミトコンドリアの活性酸素と酸素消費量の増加は、カエンフェロール処理によって安定化されました。
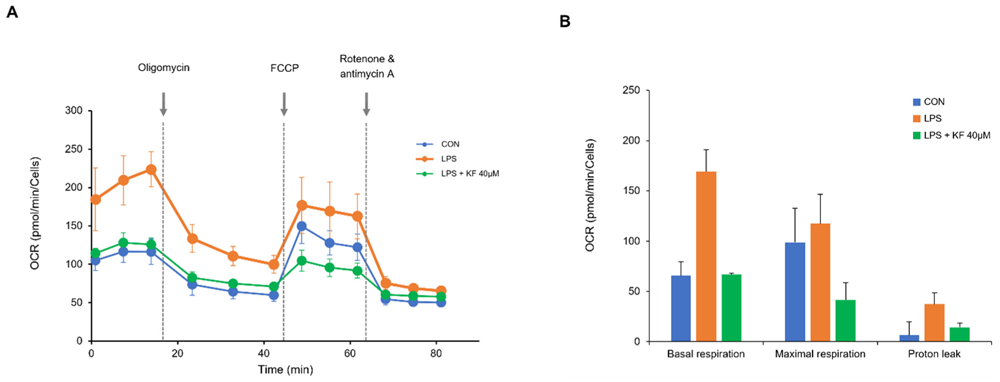
Figure:酸素消費に対するカエンフェロールとLPSの影響。OCRは代謝アナライザーを用いてリアルタイムで測定し、ミトコンドリア呼吸阻害剤を順次注入した。(A)LPSで処理した前立腺オルガノイドとカエンフェロールを併用した前立腺オルガノイドの酸素消費速度。LPS誘導群では、FCCP注入後に観察された最大OCRに比べ、基礎OCRは28%増加した。カエンフェロールとLPSの共投与は、OCRをコントロールレベルまで減少させた。(B)OCR測定により、基礎呼吸、最大呼吸、プロトンリークを同時に測定した。データは4つの独立した実験からの平均±SDを表す。興味深いことに、LPS処理により最大呼吸能が低下したため、LPS処理群ではプロトンリークが高くなった。これはLPSによるミトコンドリア損傷の徴候と考えられる。
Reference:Kaempferol Alleviates Mitochondrial Damage by Reducing Mitochondrial Reactive Oxygen Species Production in Lipopolysaccharide-Induced Prostate Organoids Myeong Joon Lee et al., Foods 2023, 12(20), 3836; https://doi.org/10.3390/foods12203836 (

)
腎淡明細胞がん(Clear cell renal cell carcinoma; ccRCC)は腎がんの最も一般的なサブタイプです。大規模なメタボロームデータは、代謝の変化と腎がんの病態および進行とを関連付けており、一部の患者ではミトコンドリア活性と生存率の低下とを相関させています。本研究の目的は、薬物反応のアバターとして患者由来のオルガノイドを用い、ミトコンドリア-リソソーム相互作用を標的とすることが新規治療アプローチとなりうるかどうかを明らかにすることでした。
本研究から、P2XR4を発現しているccRCC細胞のサブセットにおいて、腫瘍由来のATPの主な供給源が酸化的リン酸化であり、腫瘍のエネルギー代謝とミトコンドリア活性に重要な影響を及ぼしていることが示唆されました。薬理学的阻害またはP2XR4サイレンシングによって誘導される長期のミトコンドリア障害は、酸素ラジカル種の増加、ミトコンドリア透過性の変化(すなわち、遷移孔複合体の開口、膜電位の消失、カルシウム過負荷)と関連していました。患者由来のオルガノイドにおいてミトコンドリア活性が高いことは、P2XR4阻害に対する感受性が高く、異種移植モデルにおいて腫瘍が縮小することと関連していました。
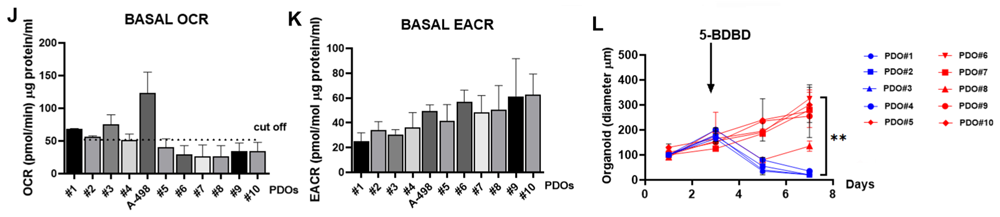
J. Seahorse XF96アナライザーで測定したPDO #1-10または親株A-498細胞の酸素消費速度(OCR)。データは生物学的4replicateの代表値。OCRの選択カットオフ値を線で示す。K. PDOと親株A-498細胞における基礎細胞外酸性化速度(ECAR)。データは生物学的4replicateの代表値。L. 5-BDBD処理後のPDOの直径。赤線はミトコンドリア活性の高いPDO、青線はミトコンドリア活性の低いPDO。データは20 replicateの平均値と±SDで報告されている。有意性は対応のないスチューデントのt検定で決定した。**, p < 0.01
Therapeutic targeting of P2X4 receptor and mitochondrial metabolism in clear cell renal carcinoma models
Christofer Rupert et al., J Exp Clin Cancer Res. 2023 May 26;42(1):134. doi: 10.1186/s13046-023-02713-1. https://jeccr.biomedcentral.com/articles/10.1186/s13046-023-02713-1 (

)
Metabolism of parathyroid organoids
Konjeti R. Sekhar et al., Front. Endocrinol., 10 July 2023 Sec. Experimental Endocrinology Volume 14 - 2023 | https://doi.org/10.3389/fendo.2023.1223312 (

)
Obesogenic diet leads to luminal overproduction of the complex IV inhibitor H2S and mitochondrial dysfunction in mouse colonocytes
Thomas Guerbette et al., FASEB J. 2023 Apr;37(4):e22853. doi: 10.1096/fj.202201971R (

)
Protocols to culture and harvest hepatic tumor organoids for metabolic assays
Man Tong et al., STAR Protoc. 2022 Jul 31;3(3):101597. doi: 10.1016/j.xpro.2022.101597 (

)
Protocol to profile the bioenergetics of organoids using Seahorse
Marlies C. Ludikhuize et al., STAR Protoc. 2021 Mar 18;2(1):100386. doi: 10.1016/j.xpro.2021.100386 (

)
Transcriptomic Landscape and Functional Characterization of Induced Pluripotent Stem Cell–Derived Cerebral Organoids in Schizophrenia
Annie Kathuria et al., JAMA Psychiatry. 2020 Jul; 77(7): 745–754. Published online 2020 Mar 18. doi: 10.1001/jamapsychiatry.2020.0196 (

)
Immune-evasive human islet-like organoids ameliorate diabetes
Eiji Yoshihara et al., Nature. 2020 Oct;586(7830):606-611. doi: 10.1038/s41586-020-2631-z. Epub 2020 Aug 19. (

)
Fine tuning the extracellular environment accelerates the derivation of kidney organoids from human pluripotent stem cells
Elena Garreta et al., Nat Mater. 2019 April ; 18(4): 397–405. doi:10.1038/s41563-019-0287-6. (

)
Integrative multi-omics analysis of intestinal organoid differentiation
Rik Gh Lindeboom et al., Mol Syst Biol. 2018 Jun 26;14(6):e8227. doi: 10.15252/msb.20188227. (

)
Integration of Sensors in Gastrointestinal Organoid Culture for Biological Analysis
Ge-Ah Kim et al., Cell Mol Gastroenterol Hepatol. 2018 Mar 26;6(1):123-131.e1. doi: 10.1016/j.jcmgh.2018.03.002. eCollection 2018. (

)
Adipocyte p62/SQSTM1 Suppresses Tumorigenesis through Opposite Regulations of Metabolism in Adipose Tissue and Tumor
Jianfeng Huang et al., Cancer Cell. 2018 Apr 9;33(4):770-784.e6. doi: 10.1016/j.ccell.2018.03.001. (

)
Organoids model distinct Vitamin E effects at different stages of prostate cancer evolution
Rose N Njoroge et al., Sci Rep. 2017 Nov 24;7(1):16285. doi: 10.1038/s41598-017-16459-2. (

)
Functional screening in human cardiac organoids reveals a metabolic mechanism for cardiomyocyte cell cycle arrest
Richard J Mills et al., Proc Natl Acad Sci U S A. 2017 Oct 3;114(40):E8372-E8381. doi: 10.1073/pnas.1707316114. Epub 2017 Sep 15. (

)
Ductal pancreatic cancer modeling and drug screening using human pluripotent stem cell- and patient-derived tumor organoids
Ling Huang et al., Nat Med. 2015 Nov;21(11):1364-71. doi: 10.1038/nm.3973. Epub 2015 Oct 26. (

)