メルクでは、SMC
®技術を利用した高感度バイオマーカー検出機器として、Erenna
®プラットフォームを数年間にわたりご提供し、信頼をいただいてきました。
SMCxPRO
®プラットフォームはErenna
®と同等の検出感度を有しながら、コンパクトさと導入コストの低減を実現しています。Erenna
®と共通の高度に検証された多種類のイムノアッセイキット、ならびに、お客様のニーズに合ったアッセイ開発サービスをご利用いただけます。
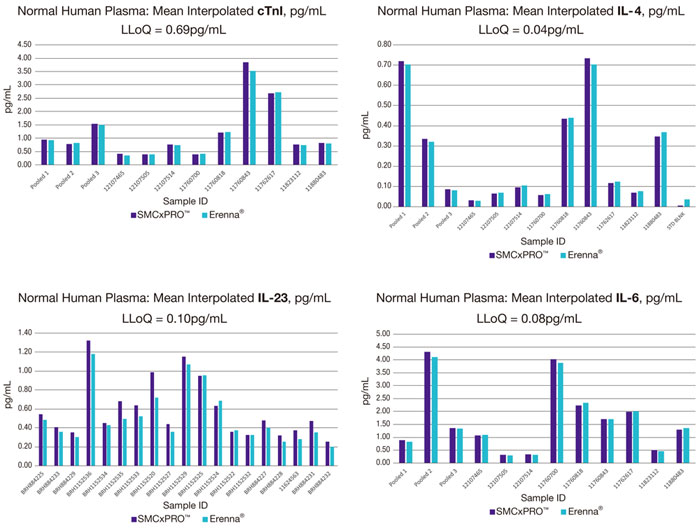
4 種のイムノアッセイキットを用いて処理した各血漿サンプルを、SMCxPRO
®とErenna
®プラットフォーム双方で計測しました。
計測した全4 グループの検体において、各サンプル濃度の平均補正(R2) は2つの機器間でほぼ同等でした。
ヒトcTnI(製品型式:03-0092-00):R2=0.9944、ヒト IL- 6(製品型式:03-0089-01):R2=0.9972、
ヒト IL- 4(製品型式:03-0052-00):R2=0.9976、ヒト IL-23(製品型式:03-0112-00):R2=0.9413。
これらの結果は、SMCxPRO
®ではErenna
®と類似した結果が得られ、Erenna
®からSMCxPRO
®へと自信をもって移行できることを証明します。
SMC
®技術を利用した研究成果論文が多数報告されています。
心血管・腎臓学
Anthracyclines and Biomarkers of Myocardial Injury (

)
Michael Mallouppas et al., JACC: CardioOncology, Available online 2 May 2023
Biological variation of cardiac myosin-binding protein C in healthy individuals (

)
Bashir Alaour et al., Clinical Chemistry and Laboratory Medicine, Published Online 23 June, 2021
Cardiovascular biomarkers in patients with COVID-19 (

)
Christian Mueller et al., European Heart Journal, Published 28 February 2021
Clinical determinants of plasma cardiac biomarkers in patients with stable chest pain. (

)
Bing R et al., Heart. 2019 Nov; Volume 105, Issue 22
Variation in renal responses to exercise in the heat with progressive acclimatization. (

)
Jessica Omassoli et al., Journal of Science and Medicine in Sport, Volume 22, Issue 9, September 2019, Pages 1004-1009
Cardiac Myosin-Binding Protein C to Diagnose Acute Myocardial Infarction in the Pre-Hospital Setting. (

)
Kaier TE et al., J Am Heart Assoc. 2019 Aug 6;8(15):e013152. doi: 10.1161/JAHA.119.013152. Epub 2019 Jul 26.
内分泌・肥満・代謝

(SMCxPRO使用)
A catecholamine-independent pathway controlling adaptive adipocyte lipolysis (

)
X Zhang et al., Nat Metab. 2026 Jan;8(1):96-115.
Removal of epididymal visceral adipose tissue prevents obesity-induced multi-organ insulin resistance in male mice (

)
Michael P Franczyk et al., Journal of the Endocrine Society Published: 20 February 2021
Alterations in pancreatic islet cell function in response to small bowel resection. (

)
Cathleen M Courtney et al., Am J Physiol Gastrointest Liver Physiol, 2020 May 28. doi: 10.1152/ajpgi.00282.2019. Online ahead of print.
Relationships of iron metabolism with insulin resistance and glucose levels in young and healthy adults. (

)
Krisai P., Eur J Intern Med. 2016 Jul;32:31-7. doi: 10.1016/j.ejim.2016.03.017. Epub 2016 Apr 21.
肝疾患
(SMCxPRO使用)
Highly sensitive single-molecule counting technology for cytokeratin 18 detection in non-alcoholic fatty liver disease using novel antibodies (

)
Pengxiang Liu et al., Microchemical Journal Volume 198, March 2024, 110155
神経疾患・腫瘍

(SMCxPRO使用)
Anti‐amyloid antibody equilibrium binding to Aβ aggregates from human Alzheimer's disease brain (

)
KD Bjørnholm et al., Alzheimers Dement. 2026 Apr;22(4):e71350.

(SMCxPRO使用)
Novel Monoclonal Antibody Detects Small Aβ Oligomers More Sensitively Than Lecanemab in Alzheimer's Disease CSF, Serum and Culture Media (

)
YR Xu et al., Ann Neurol. 2026 Mar 16.
An improved immunoassay detects Aβ oligomers in human biofluids: their CSF levels rise with tau and phosphotau levels (

)
Ting Yang et al., Alzheimers Res Ther. 2025 Jul 12;17(1):153. doi: 10.1186/s13195-025-01802-x.
(SMCxPRO使用)
Lecanemab-Associated Amyloid-β Protofibril in Cerebrospinal Fluid Correlates with Biomarkers of Neurodegeneration in Alzheimer’s Disease (

)
M Noguchi-Shinohara et al., Ann Neurol. 2025 Jan 6. doi: 10.1002/ana.27175.
(SMCxPRO使用)
Micromotor-based electrochemical immunoassays for reliable determination of amyloid-β (1-42) in Alzheimer's diagnosed clinical samples (

)
José M Gordón Pidal et al., Biosens Bioelectron. 2024 Apr 1:249:115988. doi: 10.1016/j.bios.2023.115988.
(SMCxPRO使用)
Lower Plasma Amyloid Beta - 42 Levels Associated With Worse Survival in Patients With Glioma (

)
Kyeongjin Seo et al., In Vivo. 2024 Jan-Feb;38(1):425-430. doi: 10.21873/invivo.13455.
Tau seed amplification assay reveals relationship between seeding and pathological forms of tau in Alzheimer’s disease brain (

)
Bryan Frey et al., Acta Neuropathologica Communications volume 11, Article number: 181 (2023)
(SMCxPRO使用)
Nasal administration of anti-CD3 monoclonal antibody ameliorates disease in a mouse model of Alzheimer’s disease (

)
Juliana R. Lopes et al., Proc Natl Acad Sci U S A. 2023 Sep 12;120(37):e2309221120. doi: 10.1073/pnas.2309221120.
(SMCxPRO使用)
A highly sensitive and quantitative assay for dystrophin protein using Single Molecule Count Technology (

)
Misawa Niki Ishii et al., Neuromuscular Disorders, Available online 23 August 2023
Anxiety adds the risk of cognitive progression and is associated with axon/synapse degeneration among cognitively unimpaired older adults (

)
Lin Sun et al., EBioMedicine. 2023 Aug;94:104703
(SMCxPRO使用)
Pharmacological PINK1 activation ameliorates Pathology in Parkinson’s Disease models (

)
Randall M. Chin et al., bioRxiv, Posted February 15, 2023.
AAV5-miHTT-mediated huntingtin lowering improves brain health in a Huntington’s disease mouse model (

)
Sarah B Thomson et al., Brain, Published: 12 December 2022
A study of the longitudinal changes in multiple cerebrospinal fluid and volumetric magnetic resonance imaging biomarkers on converter and non-converter Alzheimer’s disease subjects with consideration for their amyloid beta status (

)
Ulyana Morar et al., Alzheimer's & Dementia, Published online: 4 February 2022
(SMCxPRO使用)
Serum amyloid beta-42 as a noninvasive biomarker for the prognosis and histologic features of glioma (

)
K Hwang et al., Journal of Neuro-oncology Posted 26 Aug, 20212021
Intrastriatal Administration of AAV5-miHTT in Non-Human Primates and Rats Is Well Tolerated and Results in miHTT Transgene Expression in Key Areas of Huntington Disease Pathology (

)
Elisabeth A. Spronck et al., Brain Sci. 20 January 2021
Cognitively normal APOE ε4 carriers have specific elevation of CSF SNAP-25 (

)
Omar H. Butt et al., Neurobiology of Aging Available online 11 February 2021
TBK1 phosphorylates mutant Huntingtin and suppresses its aggregation and toxicity in Huntington's disease models. (

)
Ramanath Narayana Hegde et al., EMBO J (2020) e104671
Target engagement in an alzheimer trial: Crenezumab lowers amyloid β oligomers in cerebrospinal fluid. (

)
Yang T et al., Ann Neurol. 2019 Jun 5. doi: 10.1002/ana.25513. [Epub ahead of print]
がん・腫瘍

(SMCxPRO使用)
Development and validation of highly sensitive ligand binding assay to measure soluble DLL3 concentration in human serum (

)
M Nishidate et al., 2025 Jun;17(11):725-736.
炎症・免疫

(SMCxPRO使用)
Phase 1 study of balinatunfib, an oral inhibitor of TNFR1 signal in mild‐to‐moderate psoriasis (

)
N Nassr et al., J Eur Acad Dermatol Venereol. 2026 Feb 11.

(SMCxPRO使用)
Icotrokinra induces early and sustained pharmacodynamic responses in phase IIb study of patients with moderate-to-severe psoriasis (

)
D Strawn et al., JCI Insight. 2025 Dec 22;10(24):e193563.
(SMCxPRO使用)
Effect of guselkumab on serum biomarkers in patients with active psoriatic arthritis and inadequate response to tumor necrosis factor inhibitors: results from the COSMOS phase 3b study (

)
Georg Schett et al., Arthritis Research & Therapy volume 25, Article number: 150 (2023)
Effect of guselkumab on serum biomarkers in Japanese palmoplantar pustulosis patients in a randomized phase 3 study (

)
Akimichi Morita et al., JEADV Clinical Practice, First published: 07 December 2022
Tralokinumab treatment improves the skin microbiota by increasing the microbial diversity in adults with moderate-to-severe atopic dermatitis: analysis of microbial diversity in ECZTRA 1, a randomized controlled trial (

)
Lisa A. Beck et al., Journal of the American Academy of Dermatology, Available online 5 December 2022
Biological impact of iberdomide in patients with active systemic lupus erythematosus (

)
Peter E Lipsky et al., Annals of the Rheumatic Diseases, First published April 27, 2022
Target engagement of the first-in-class CXCR7 antagonist ACT-1004-1239 following multiple-dose administration in mice and humans (

)
Christine Huynh et al., Biomedicine & Pharmacotherapy Available online 28 October 2021
Early quantification of systemic inflammatory-proteins predicts long-term treatment response to Tofacitinib and Etanercept: Psoriasis response predictions using blood. (

)
Lewis E. Tomalin et al., Journal of Investigative Dermatology, In press, journal pre-proof, Available online 6 November 2019
Asian atopic dermatitis serum is characterized by Th2/Th22-activation, highly correlated with non-lesional skin measures. (

)
Huei-Chi Wen et al., Journal of Allergy and Clinical Immunology, Volume 142, Issue 1, July 2018, Pages 324-328.e11
呼吸器・睡眠医学
Subclinical sleep apnoea and plasma levels of endothelin-1 among young and healthy adults. (

)
Schoen T et al., Open Heart. 2017 Mar 1;4(1):e000523. doi: 10.1136/openhrt-2016-000523. eCollection 2017.
老化
A dual MTOR/NAD+ acting gerotherapy (

)
Jinmei Li et al., bioRxiv, Posted January 19, 2023.
創薬
(SMCxPRO使用)
Utilizing PK and PD Biomarkers to Guide the First-in-Human Starting Dose Selection of MTBT1466A: A Novel Humanized Monoclonal Anti-TGFb3 Antibody for the Treatment of Fibrotic Diseases(

)
Rajbharan Yadav et al., J Pharm Sci. 2023 Jul 8;S0022-3549(23)00279-4.
(SMCxPRO使用)
The Development and Characterization of a Highly Sensitive Mature TGFβ3 Assay to Evaluate Anti-TGFβ3 Target Engagement (

)
A. Francesca Setiadi et al., The AAPS Journal volume 25, Article number: 21 (2023)
SMCxPRO®技術紹介
Quantitation of low abundant soluble biomarkers using high sensitivity Single Molecule Counting technology. (

)
Joseph Hwang et al., Methods, Volume 158, 1 April 2019, Pages 69-76
Combining single molecule counting with bead-based multiplexing to quantify biological inflammation time course following skeletal muscle injury. (

)
Elizabeth A.Tanner et al., Methods, Volume 158, 1 April 2019, Pages 77-80
※上記の他にも多数の論文がございます。詳細はお問合わせください。